Alimentos transgénicos: qué son y cómo se obtienen
Descárgate aquí el PDF sobre métodos de obtención de alimentos transgénicos
Los alimentos transgénicos constituyen una de las aplicaciones más conocidas de la biotecnología vegetal y, al mismo tiempo, una de las que más interés ha despertado tanto en el ámbito científico como en el social.
Su desarrollo parte de la posibilidad de modificar genéticamente plantas destinadas a la alimentación para incorporar rasgos concretos de interés agronómico, nutricional o tecnológico.
Esto ha permitido abrir nuevas líneas de trabajo orientadas a mejorar la resistencia de los cultivos, optimizar determinadas características de los alimentos y explorar soluciones frente a algunos de los retos actuales de la producción agrícola. Sin embargo, su utilización también ha generado preguntas sobre su obtención, su utilidad real y las limitaciones que presentan.
Por ello, para entender el papel que ocupan dentro de la biotecnología vegetal, conviene analizar primero qué son los alimentos transgénicos, cómo se obtienen y cuáles son sus principales ventajas y desventajas.
Qué son los alimentos transgénicos
En biotecnología vegetal, los alimentos transgénicos son aquellos obtenidos a partir de plantas modificadas mediante ingeniería genética para introducir genes de otra especie.
Estas plantas, consideradas organismos genéticamente modificados (OGM), pueden incorporar características de interés agronómico o alimentario, como una mayor resistencia a plagas, una composición nutricional mejorada o tolerancia a herbicidas.
Ejemplos de alimentos transgénicos
Algunos ejemplos de modificaciones genéticas aplicadas a alimentos en distintos países son los siguientes:
- Maíz: en Estados Unidos se han desarrollado variedades con resistencia a determinados insectos y tolerancia a herbicidas.
- Soja: en Estados Unidos se han autorizado variedades con tolerancia a herbicidas y, en algunos casos, con modificaciones en la composición del aceite para mejorar su perfil nutricional.
- Canola o colza: en Canadá se han aprobado líneas con tolerancia al glifosato, lo que facilita el control químico de malas hierbas durante el cultivo.
- Papaya: en Estados Unidos se introdujeron variedades con resistencia al virus de la mancha anular, una modificación especialmente relevante para la producción en Hawái.
- Manzana: en Estados Unidos se han desarrollado variedades diseñadas para retrasar el pardeamiento tras el corte o el golpe, lo que mejora su conservación y presentación comercial.
- Patata: en Estados Unidos se han autorizado variedades con menor pardeamiento y con resistencia a determinadas plagas o enfermedades.
- Piña: en Estados Unidos se comercializa una variedad modificada para aumentar el contenido de licopeno, responsable de su color rosado.
- Arroz: en Filipinas se aprobó el llamado Golden Rice, desarrollado para incrementar el contenido de provitamina A.
Todos estos ejemplos muestran que la biotecnología vegetal no se limita a modificar genes de forma aislada, sino que permite desarrollar soluciones concretas frente a problemas agronómicos, nutricionales y productivos. Comprender cómo se diseñan, evalúan y aplican estas estrategias resulta clave para interpretar el papel actual de la mejora genética en agricultura y alimentación. En este contexto, el Máster en Biotecnología Vegetal de la UNIA ofrece una formación especializada para profundizar en las herramientas, metodologías y aplicaciones que están transformando este campo.
Máster en biotecnología vegetal
Cómo se obtienen los alimentos transgénicos vegetales
La obtención de alimentos transgénicos requiere la aplicación de distintos métodos y herramientas de ingeniería genética.
En este proceso, no solo intervienen técnicas para introducir material genético en las células vegetales, sino también herramientas que permiten modificarlo o incorporarlo de forma dirigida.
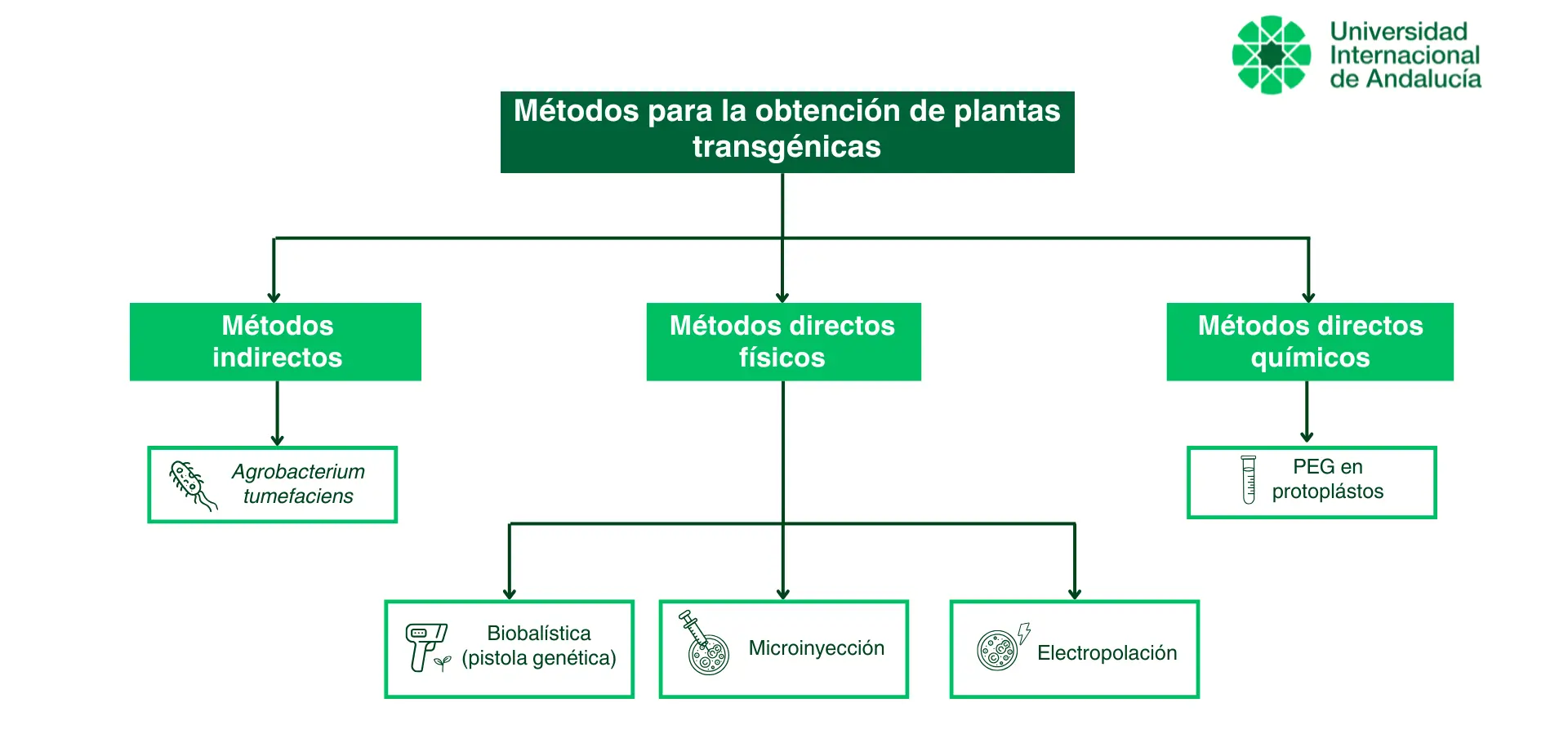
1. Métodos indirectos o mediados por vectores
Los métodos indirectos o mediados por vectores utilizan sistemas biológicos para introducir material genético en las células vegetales.
A diferencia de los métodos directos, no transfieren el ADN por medios físicos o químicos, sino a través de un organismo capaz de actuar como vehículo biológico.
Transformación mediada por Agrobacterium tumefaciens
La transformación mediada por Agrobacterium tumefaciens es uno de los métodos más utilizados en biotecnología vegetal.
Aprovecha la capacidad natural de esta bacteria para transferir un fragmento de ADN a las células vegetales. En el laboratorio, ese sistema se modifica para sustituir los genes responsables de la patogenicidad por el gen de interés, que se inserta en la región transferible del plásmido.
Una vez transferido, ese ADN puede integrarse en el genoma de la planta y dar lugar, tras selección y regeneración in vitro, a una planta transformada.
2. Métodos directos físicos
Los métodos directos físicos introducen ADN desnudo en las células vegetales sin recurrir a vectores biológicos.
Para ello, utilizan procedimientos mecánicos o eléctricos que permiten que el material genético atraviese la pared y la membrana celular y alcance el interior de la célula.
Dentro de este grupo, la biobalística ha sido uno de los métodos más utilizados, especialmente en especies que en los primeros desarrollos resultaban poco susceptibles a la transformación mediante sistemas biológicos.
Biobalística (pistola genética)
La biobalística consiste en bombardear el tejido vegetal con micropartículas de oro o tungsteno recubiertas con el ADN de interés. Estas partículas se aceleran a gran velocidad, normalmente mediante gases a alta presión, y atraviesan la pared y la membrana celular.
Una vez dentro de la célula, el ADN puede desprenderse de la partícula e integrarse en el genoma vegetal, lo que permite obtener células transformadas y, posteriormente, regenerar plantas completas.
Microinyección
La microinyección es un método directo físico que consiste en introducir el ADN de interés de forma puntual en una célula vegetal mediante una micropipeta de diámetro muy fino.
A diferencia de la biobalística, donde el material genético se dispersa sobre un conjunto de células, aquí la transferencia se realiza célula a célula y bajo control microscópico.
En plantas, su aplicación se ha orientado sobre todo a protoplastos, cigotos o células aisladas, ya que la pared celular dificulta la penetración directa de la micropipeta.
Por ese motivo, aunque se ha utilizado en sistemas vegetales y sigue teniendo interés experimental, su uso es mucho más limitado que el de otros métodos de transformación más escalables.
Electroporación
La electroporación es un método directo físico basado en la aplicación de pulsos eléctricos breves y de alto voltaje que alteran el potencial de membrana y generan poros transitorios.
A través de estos poros, el ADN puede atravesar la membrana e incorporarse al interior celular. En transformación vegetal, esta técnica se aplica sobre todo a protoplastos, donde la ausencia de pared celular mejora la eficiencia del proceso.
3. Métodos directos químicos
Los métodos directos químicos introducen ADN en las células vegetales sin recurrir a vectores biológicos.
Para ello, emplean compuestos que favorecen la entrada del material genético a través de la membrana celular.
PEG en protoplastos
La transformación con PEG es un método directo químico que se aplica sobre todo a protoplastos, es decir, células vegetales a las que se les ha eliminado la pared celular.
En este sistema, el ADN de interés se mezcla con los protoplastos en presencia de polietilenglicol (PEG) y de cationes divalentes. El PEG favorece que el ADN precipite sobre la superficie de la membrana del protoplasto y, a partir de ahí, ese material genético pueda introducirse en la célula.
Después, si la transformación tiene éxito, los protoplastos pueden cultivarse y regenerar tejidos o plantas completas.
¿Quieres ver cómo se aplican estos métodos en investigación real?
Hemos preparado un PDF en el que se explican en mayor profundidad los principales métodos de obtención de alimentos transgénicos y se presentan casos de estudio reales.
Descárgalo rellenando el formulario que encontrarás a tu izquierda.
Herramientas para la edición genética
Además de los métodos utilizados para introducir ADN en las células vegetales, la biotecnología dispone de herramientas que permiten modificar el material genético de forma más precisa.
Estas herramientas actúan sobre secuencias concretas del genoma y permiten cortar, eliminar, sustituir o regular fragmentos de ADN, lo que ha ampliado las posibilidades de la mejora vegetal y ha dado lugar a nuevas estrategias de modificación genética.
1. CRISPR-Cas9
CRISPR-Cas9 es una herramienta de edición genética que permite modificar secuencias concretas del ADN vegetal con un alto grado de precisión.
Su funcionamiento se basa en la acción conjunta de un ARN guía, que dirige el sistema hacia la región diana del genoma, y de la nucleasa Cas9, que realiza un corte en ese punto.
A partir de esa rotura, los mecanismos de reparación de la célula pueden dar lugar a la modificación genética deseada.
2. TALENs
Las TALENs (Transcription Activator-Like Effector Nucleases) son herramientas de edición genética diseñadas para reconocer y cortar secuencias concretas del ADN.
Están formadas por dos partes: un dominio de unión al ADN, derivado de proteínas TALE, que reconoce la secuencia diana, y un dominio nucleasa, encargado de realizar el corte.
Cuando la TALEN se une al fragmento de ADN seleccionado, la nucleasa se activa y genera una rotura en ese punto del genoma. A partir de ahí, la célula repara el ADN y puede producirse la modificación genética deseada.
3. ZFN
Las ZFN (Zinc Finger Nucleases) son herramientas de edición genética diseñadas para generar roturas de doble cadena en secuencias específicas del ADN. Están formadas por un dominio de unión al ADN basado en dedos de zinc, que reconoce la región diana, y un dominio nucleasa, que realiza el corte.
A partir de esa rotura, la célula activa sus mecanismos de reparación, lo que permite introducir mutaciones, deleciones o modificaciones dirigidas en el genoma.
Ventajas y desventajas de los alimentos transgénicos
Una vez explicados los principales métodos y herramientas empleados en su obtención, conviene analizar qué ventajas pueden aportar estas modificaciones.
En este contexto, el desarrollo de alimentos transgénicos se ha asociado a distintos beneficios agronómicos, nutricionales y tecnológicos. Su interés radica en la posibilidad de mejorar determinados rasgos de los cultivos y de los alimentos obtenidos a partir de ellos, tanto en términos de producción como de calidad.
|
Ventajas |
|
|
Resistencia a herbicidas |
Permite desarrollar cultivos capaces de tolerar determinados herbicidas, lo que facilita el control de malas hierbas y simplifica parte del manejo agronómico. |
|
Mayor resistencia a plagas, insectos y algunos virus |
Algunos cultivos transgénicos incorporan rasgos de resistencia frente a insectos o enfermedades, lo que puede reducir pérdidas de cosecha y, en determinados contextos, disminuir el uso de insecticidas. |
|
Mejora nutricional |
La modificación genética también puede orientarse a aumentar o cambiar compuestos de interés nutricional. Un ejemplo conocido es el arroz enriquecido con provitamina A. |
|
Reducción o silenciamiento de componentes alergénicos |
En algunos desarrollos, la ingeniería genética puede dirigirse a reducir proteínas alergénicas concretas, con el objetivo de generar alimentos potencialmente menos problemáticos para personas sensibles. |
|
Mayor conservación poscosecha |
La modificación genética puede orientarse a retrasar el pardeamiento o el deterioro tras la cosecha, lo que mejora la conservación del alimento y puede contribuir a reducir el desperdicio. |
|
Tolerancia a sequía, salinidad u otros estreses ambientales |
Algunos desarrollos buscan que el cultivo soporte mejor condiciones adversas, lo que amplía su interés en contextos de cambio climático o en zonas con limitaciones ambientales. |
Sin embargo, su desarrollo y uso también plantean limitaciones que deben analizarse con detalle.
Estas no solo se relacionan con la seguridad y la evaluación científica de cada producto, sino también con sus posibles efectos sobre el medio ambiente, la aparición de resistencias y la complejidad regulatoria que acompaña a este tipo de tecnologías.
|
Desventajas |
|
|
Posibles efectos sobre la salud deben evaluarse caso por caso |
Cada alimento transgénico debe someterse a una evaluación específica para descartar problemas de toxicidad, alergenicidad o cambios no deseados en su composición. |
|
Preocupación por alergenicidad |
La introducción de nuevas proteínas obliga a estudiar si pueden comportarse como alérgenos o si presentan similitudes con proteínas alergénicas ya conocidas. |
|
Preocupación por toxicidad o cambios imprevistos |
También se analiza si la modificación genética puede producir efectos tóxicos no deseados o alterar el perfil nutricional del alimento de forma relevante. |
|
Posible transferencia de genes marcadores de resistencia a antibióticos |
Es una preocupación histórica en bioseguridad, ya que se estudia la posibilidad de que determinados genes marcadores puedan transferirse a microorganismos. |
|
Aparición de resistencias en malas hierbas o plagas |
El uso continuado de cultivos tolerantes a herbicidas o resistentes a insectos puede favorecer la selección de malas hierbas o insectos resistentes, reduciendo parte de la ventaja inicial. |
|
Impactos ecológicos y sobre la biodiversidad |
Entre las limitaciones más debatidas se encuentran el flujo génico, los cambios en comunidades biológicas y el posible efecto sobre la diversidad agrícola y ecológica. |
|
Mayor complejidad regulatoria y analítica |
A medida que los productos expresan más proteínas nuevas o combinan varios rasgos, su evaluación de seguridad resulta más compleja y exige metodologías cada vez más precisas. |
|
Coste y dependencia tecnológica |
La adopción de estas semillas puede implicar mayores costes de acceso, licencias o dependencia de proveedores tecnológicos, lo que introduce una limitación económica y estructural. |
Referencias
Acosta-Losada, O., & Guerrero-Fonseca, C. A. (2007). Alimentos transgénicos y alergenicidad. Revista de la Facultad de Medicina, 55(4), 251–269.
Agència Catalana de Seguretat Alimentària. (2023). Avaluació de la seguretat dels organismes modificats genèticament (OMG). https://scientiasalut.gencat.cat/bitstream/handle/11351/10504/avaluacio_seguretat_organismes_modificats_geneticament_omg_2023_ca.pdf?sequence=1
Bhomkar, P., Upadhyay, C. P., Saxena, M., Muthusamy, A., Prakash, N. S., Pooggin, M. M., & Kumar, P. P. (2014). Efficient transformation of oil palm protoplasts by PEG-mediated transfection and DNA microinjection. PLOS ONE, 9(5), e96831. https://doi.org/10.1371/journal.pone.0096831
Department of Agriculture, Republic of the Philippines. (s. f.). Biosafety pioneer lauds “Golden Rice” approval. https://www.da.gov.ph/biosafety-pioneer-lauds-golden-rice-approval/
European Food Safety Authority (EFSA) GMO Panel. (2025). Current practice, challenges and future opportunities in the safety assessment of newly expressed proteins in genetically modified plants. EFSA Journal. https://doi.org/10.2903/j.efsa.2025.9568
Gaj, T., Gersbach, C. A., & Barbas, C. F. III. (2013). ZFN, TALEN, and CRISPR/Cas-based methods for genome engineering. Trends in Biotechnology, 31(7), 397–405. https://doi.org/10.1016/j.tibtech.2013.04.004
Hasan, N., Choudhary, S., Naaz, N., Sharma, N., & Laskar, R. A. (2021). Recent advancements in molecular techniques of gene transfer to plants by electroporation and its applications. Molecular Biology Reports, 48, 301–315.
Health Canada. (s. f.). Novel food information: Glyphosate tolerant canola, GT73. https://www.canada.ca/en/health-canada/services/food-nutrition/genetically-modified-foods-other-novel-foods/approved-products/glyphosate-tolerant-canola-gt73.html
Hwang, H.-H., Yu, M., & Lai, E.-M. (2017). Agrobacterium-mediated plant transformation: Biology and applications. The Arabidopsis Book, 15, e0186. https://doi.org/10.1199/tab.0186
Kempken, F., & Jung, C. (2003). Plant transformation via protoplast electroporation. En Plant Functional Genomics (Methods in Molecular Biology). Humana Press.
KeyGene N.V. (2014). Un método de mutagénesis mejorada utilizando polietilenglicol por introducción de bases nitrogenadas mutagénicas en protoplastos vegetales (Patente ES2450743T3). Oficina Española de Patentes y Marcas. https://patentimages.storage.googleapis.com/1a/70/9f/ed126dcdb78c41/ES2450743T3.pdf
Luque Polo, K. (2017). Seguridad alimentaria y alimentos transgénicos. Observatorio Medioambiental, 20, 59–75.
National Academies of Sciences, Engineering, and Medicine. (2016). Genetically engineered crops: Past experience and future prospects. National Academies Press. https://doi.org/10.17226/23395
Por Qué Biotecnología / ArgenBio. (2021). Cuaderno N.º 18: Elaboración de una planta transgénica. Técnica de Agrobacterium tumefaciens. https://www.porquebiotecnologia.com.ar/Cuadernos/El_Cuaderno_18_Tecnica_de_Agrobacterium_tumefaciens.pdf
Por Qué Biotecnología / ArgenBio. (2021). Cuaderno N.º 28: Elaboración de una planta transgénica. Técnica de biobalística. https://www.porquebiotecnologia.com.ar/Cuadernos/El_Cuaderno_28_Tecnica_de_biobalistica.pdf
Takayama, M., Matsukura, C., Ariizumi, T., Ezura, H., & Nishihara, M. (2017). Efficient increase of γ-aminobutyric acid (GABA) content in tomato fruits by targeted mutagenesis. Scientific Reports, 7, 7057. https://doi.org/10.1038/s41598-017-06400-y
U.S. Food and Drug Administration. (s. f.). GMO crops, animal food, and beyond. https://www.fda.gov/food/agricultural-biotechnology/gmo-crops-animal-food-and-beyond
World Health Organization. (s. f.). Food, genetically modified. https://www.who.int/news-room/questions-and-answers/item/food-genetically-modified